




引言
在新发表的一篇医学文献中,研究人员系统梳理了靶向衰老细胞的两大前沿方向——细胞外囊泡(EVs)与免疫细胞。
细胞衰老是生物体衰老的核心标志之一。衰老细胞的积累与多种年龄相关疾病的发病机制密切相关。
研究发现,间充质干细胞来源的细胞外囊泡具有显著抗衰老潜力。细胞外囊泡中microRNA(miRNA)被证实参与衰老调控网络,例如干细胞分泌的miR-499a可下调PI3K-mTOR通路,减少生长激素诱导的衰老细胞积累。同时,科学家们正在开发利用适应性免疫清除衰老细胞的策略,如疫苗和免疫细胞疗法。
未来,基于细胞外囊泡及免疫细胞的策略有望为人类抗衰领域带来更大的突破。
衰老及年龄相关疾病是全球多发病和死亡的主要驱动因素。
细胞衰老是生物体衰老的核心标志之一。衰老细胞的积累与多种年龄相关疾病的发病机制密切相关。
近年来,针对衰老细胞的抗衰老策略备受关注。
日前,发表于《Journal of Translational Internal Medicine》的综述“Senescent cells as a target for anti-aging interventions: From senolytics to immune therapies”系统梳理了靶向衰老细胞的两大前沿方向——细胞外囊泡(EVs)疗法与免疫细胞疗法,这些策略正从实验室走向临床,为对抗衰老相关疾病提供了全新思路 [1]。
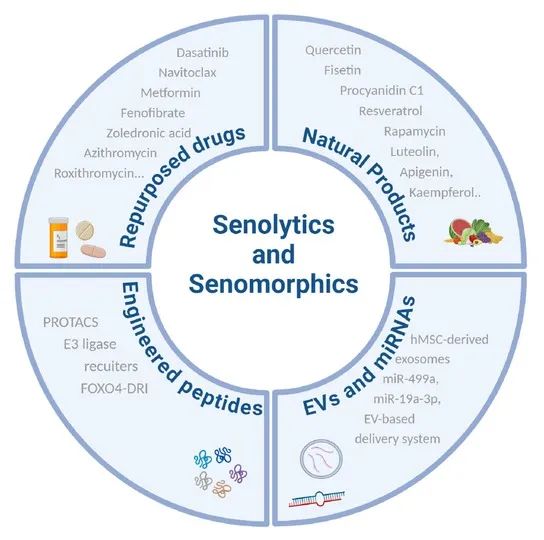
抗衰老策略,图片来自文献[1]
细胞衰老:是多种年龄相关疾病的病理基础
细胞衰老是细胞周期永久停滞的生物学过程,由端粒缩短、DNA损伤、氧化应激或癌基因激活等因素触发,是多种年龄相关疾病(如阿尔茨海默病、心血管疾病、骨关节炎)的病理基础。
其主要特征包括(图1):
形态变化:细胞扁平化、体积增大;
分子标志物:① 细胞周期抑制蛋白(p16、p21)高表达;② 溶酶体SA-β-gal活性活性升高;③ DNA损伤标记(γH2AX、53BP1)积累;④ 表观遗传改变:核膜蛋白(如lamin B1)丢失。
衰老相关表型(SASP):分泌促炎因子(IL-6、TNF-α)、趋化因子及基质金属蛋白酶,介导慢性炎症和组织功能障碍。
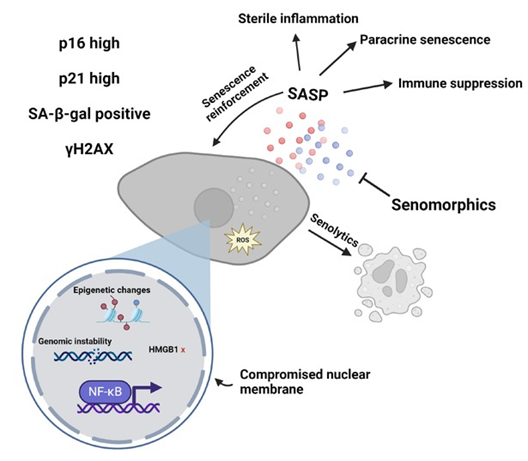
图1,细胞衰老过程中的代谢变化和抗衰老疗法的机制。细胞衰老主要表现为p16、p21、SA-β-gal、DNA损伤和促炎SASP的升高。两类化学抗衰老药物是抗衰老药物和抗衰老形态药物,它们分别促进衰老溶解和抑制SASP。
生理状态下,衰老细胞有助于伤口愈合、纤维化解决、免疫细胞募集、肿瘤发生抑制以及胚胎发生期间前肢和神经管的发育。
病理状态下,衰老细胞的积累会导致组织再生受损、慢性炎症和纤维化。SASP中的细胞因子和趋化因子还可能在周围组织中建立免疫抑制环境,促使恶性癌细胞表现出干细胞特性、免疫逃逸和转移。
细胞外囊泡(EVs):天然信号载体,重塑衰老微环境
细胞外囊泡是细胞分泌的纳米级膜结构,可携带蛋白质、核酸等生物活性分子介导细胞间通讯。
研究发现,间充质干细胞(MSCs)来源的EVs具有显著抗衰老潜力。在高糖诱导衰老的成纤维细胞中,人源MSC-EVs通过抑制RAGE受体通路、降低活性氧(ROS)水平、调控Smad信号,降低了衰老标志物p21和SA-β-gal的表达量。在Ercc1基因缺陷型早衰小鼠模型中,胚胎干细胞来源的EVs治疗使多个器官的衰老负荷降低,并延长了早衰小鼠的健康寿命。
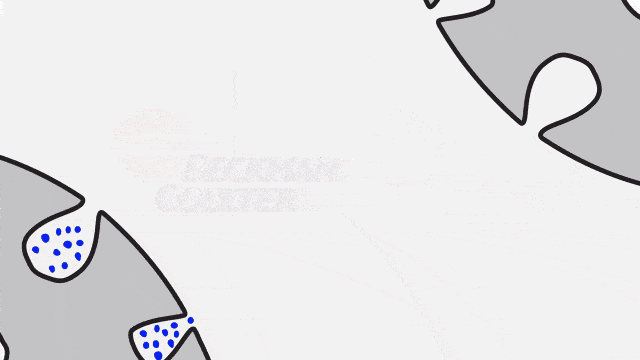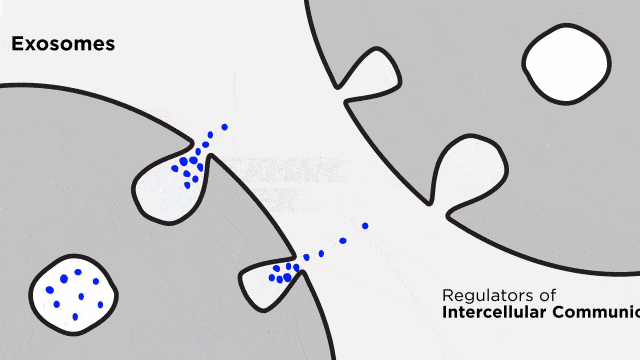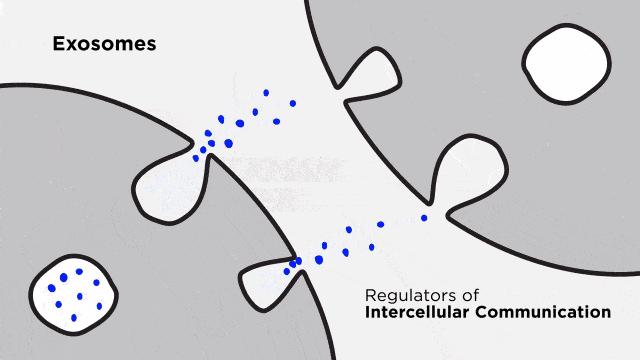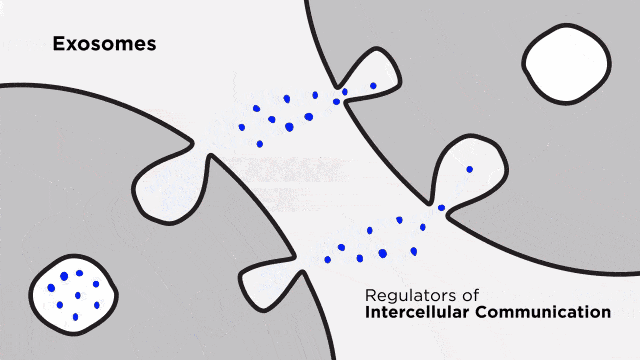
EVs内富含的microRNA(miRNA)被证实参与衰老调控网络。干细胞分泌的miR-499a可下调PI3K-mTOR通路,减少生长激素诱导的衰老细胞积累;miR-19a-3p模拟物则通过抑制p53/p21轴,降低氧化应激诱导的成骨细胞衰老率。
EVs还被用作递送载体,以增强现有抗衰老疗法的疗效。
科学家开发了工程化EVs装载技术以提高靶向性:通过表面展示抗GPNMB抗体,EVs可精准识别衰老细胞表面标志物。含有达沙替尼+槲皮素(D+Q)的EVs在消除衰老细胞方面的效率高于传统的口服给药方法。
这种天然载体系统避免了传统药物全身分布带来的副作用,为局部组织衰老干预提供了新方案。
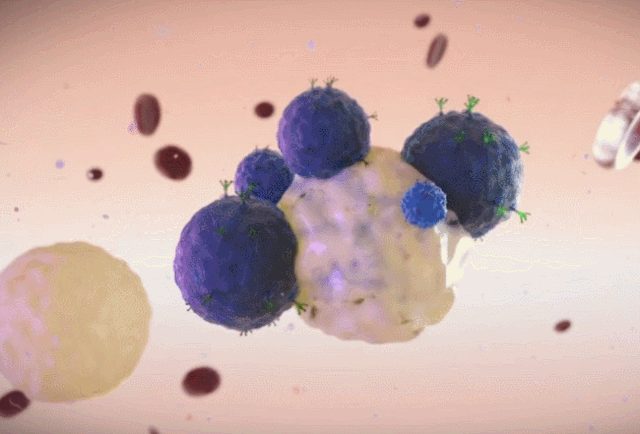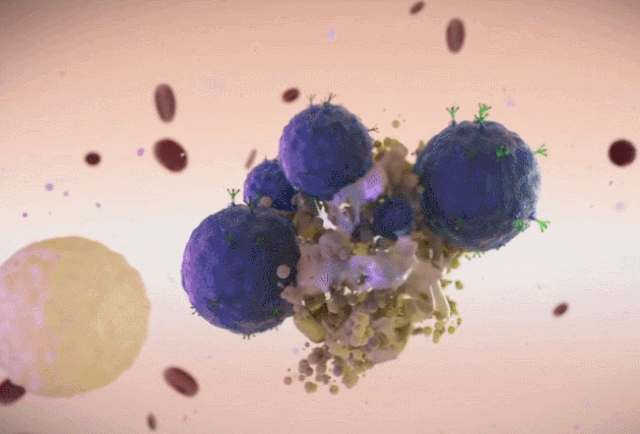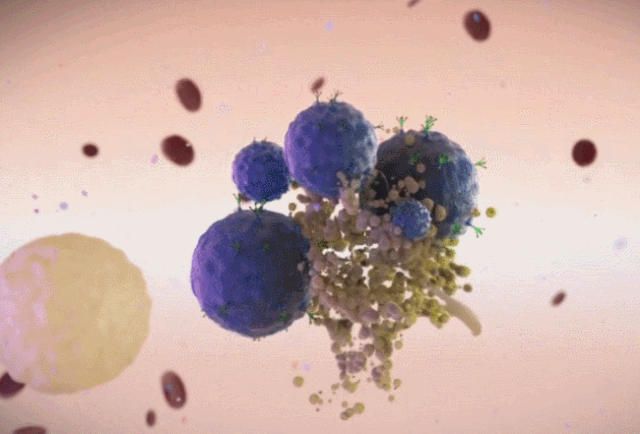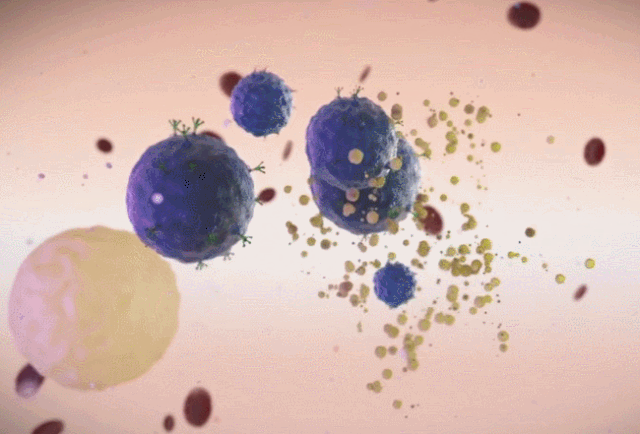
这些发现提示,基于miRNA的基因疗法可能通过调控关键节点逆转衰老表型,目前已有研究尝试通过脂质纳米颗粒实现miRNA的定向递送。
免疫细胞:靶向衰老细胞表面抗原,精准清除衰老细胞
衰老细胞的清除受到先天和适应性免疫系统的调节。然而,SASP的免疫抑制效应阻碍了免疫系统清除衰老细胞,导致它们随着年龄的增长而积累,并引发与年龄相关的疾病。
科学家们正在开发利用适应性免疫清除衰老细胞的策略,如疫苗和免疫细胞疗法。
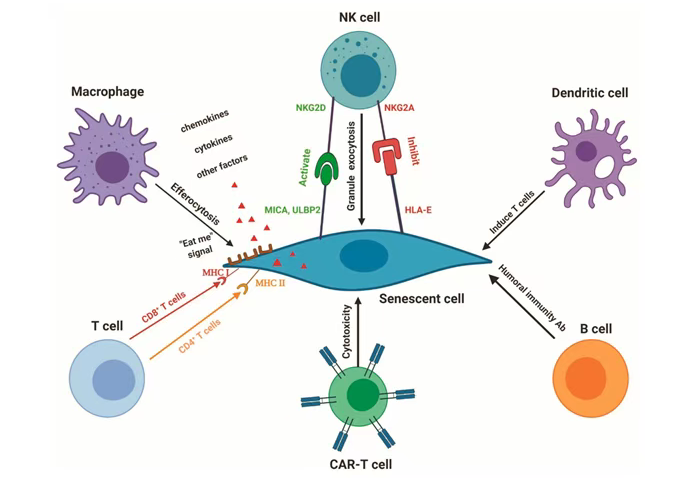
图1. 不同的衰老细胞产生不同的配体,包括 MICA/B、ULBP2、MHC I、MHC II 和 HLA-E。个体免疫细胞,包括巨噬细胞、NK 细胞、T 细胞、CAR-T 细胞和树突状细胞,可以通过这些配体精确识别衰老细胞,并靶向根除衰老细胞。B 细胞可能通过体液免疫抗体攻击衰老细胞[2]。
在肿瘤治疗中大放异彩的CAR-T技术,现被改造用于清除衰老细胞。针对衰老细胞高表达的uPAR蛋白,研究人员开发了特异性CAR-T细胞。CAR-T细胞能够绕过癌症免疫逃逸机制,并以主要组织相容性复合体(MHC)非依赖性方式消除癌细胞。
在四氯化碳诱导的肝纤维化模型中,uPAR-CAR-T治疗使肝脏胶原沉积和纤维化面积减小。更值得注意的是,年轻小鼠接受单次输注后,CAR-T细胞可在体内持续存在12个月,显著延缓年龄相关的代谢紊乱发生。
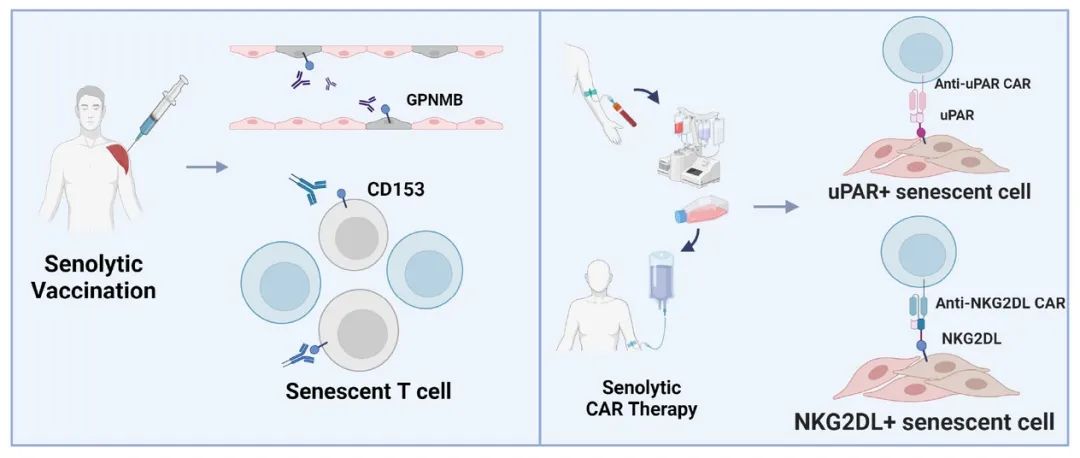
图片来自文献[1]
基于自然杀伤细胞2族成员D配体(NKG2DL)配体在衰老细胞的特异性表达,科学家构建了NKG2D-CAR-T细胞。在非人灵长类动物实验中,单次治疗即可降低多个器官的IL-6、TNF-α等炎症因子水平。与T细胞相比,CAR-NK疗法具有更低细胞因子释放风险,且可实现"现货式"生产,目前已有4项相关临床试验完成方案设计。
小结
近年来,靶向衰老细胞的治疗策略为抗衰老领域带来突破性进展。研究表明,清除或修复衰老细胞不仅能延缓年龄相关疾病的发生,更能显著提升健康寿命。其中,细胞外囊泡(EVs)和免疫细胞疗法成为两大前沿方向——干细胞来源的EVs通过携带活性物质(如miRNA)调控衰老相关信号通路;而基于疫苗、CAR-T等技术的免疫疗法则能精准识别并清除衰老细胞,从源头阻断其有害影响。未来研究需整合多学科技术,推动个性化抗衰老干预方案的开发,最终实现“健康老龄化”的目标,帮助人们在晚年依然能保持良好的身体机能和生活质量。
参考文献
1. Fu, T. & Zhou, Z. (2025). Senescent cells as a target for anti-aging interventions: From senolytics to immune therapies. Journal of Translational Internal Medicine, 13(1), 33-47.
2.Song, P., An, J., & Zou, M. H. (2020). Immune Clearance of Senescent Cells to Combat Ageing and Chronic Diseases. Cells, 9(3), 671.
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
