




近日,美国FDA药物评价与研究中心(CDER)发布了该机构2025年新药审评年度报告。报告指出,FDA在新药审评与批准方面持续保持高效与稳定的节奏,围绕疾病的预防、诊断、治疗与治愈,推动了一批具有重要临床意义的创新疗法进入临床应用。这些获批药物覆盖多个疾病领域。
2025年,CDER共批准了46款新药;若将生物制品评估与研究中心(CBER)的数据也计算在内,2025年美国共批准了58种新药。这些药物以新药申请(NDA)项下的新分子实体(NME)或生物制品许可申请(BLA)项下的新型治疗性生物制品形式获批,其活性成分此前均未获得FDA批准。2025年获批的新疗法覆盖传染病、神经系统疾病、疼痛管理、精神健康、心血管与血液疾病、肾脏与内分泌疾病、炎症、肺部疾病、过敏与免疫、肿瘤、眼科疾病以及女性健康等多个领域。
从2016年至2025年的十年数据来看,CDER平均每年批准约47款新药,2025年的批准数量与这一长期水平基本一致,反映出该机构创新药审评与批准体系的稳定输出。
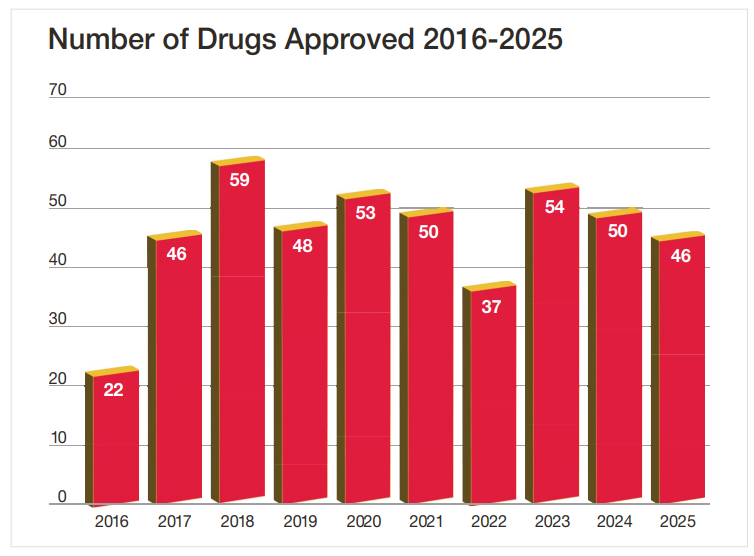
CDER批准的46款新药中小分子药物有31款,占比达67%;蛋白质类药物有12种,占比26%,在这12种蛋白质类药物中,包括7种(占总数15%)新型单克隆抗体和2种(占总数4%)ADC药物;另外还有3种(占比6%)寡核苷酸类药物。与此同时,CBER批准了5款CGT疗法、4款疫苗。
2025年CBER 批准的5款 CGT 疗法:
ITVISMA(Onasemnogene abeparvovec-brve): 2025年11月24日获批的一种基于腺相关病毒(AAV)载体的基因疗法,该疗法适用于治疗携带SMN1基因突变的2岁及以上脊髓性肌萎缩症(SMA)儿童和成人患者。
PAPZIMEOS(Zopapogene imadenovec-drba): 基于非复制腺病毒载体的免疫疗法,于2025年8月14日获批,用于治疗成人复发性呼吸道乳头状瘤病(RRP)。据悉,该疗法是全球首个且目前唯一获得FDA批准用于治疗成人RRP的疗法。
本文转载自药明康德、聊疗细胞公众号等。
相关新闻
博雅新闻
前沿动态

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
