




引言
干细胞疗法作为一种新兴技术,是再生医学、个体化医疗和细胞疗法的三位一体。其中,间充质干细胞(MSC)凭借低免疫原性、高增殖潜力以及免疫调节等特性被广泛应用研究。根据最新文献统计,截至2023年,全球已有一千多项注册临床试验使用MSC疗法, 12种MSC疗法获得监管机构批准商业化。未来,间充质干细胞将在更多疾病的治疗中发挥重要作用。
间充质干细胞具有分化为中胚层来源的各种组织的潜力,可以从多个组织中分离出来,并具有在体外扩增的能力。此外,间充质干细胞还被证明可以产生抗炎分子,从而调节细胞免疫反应。
MSC来源有两类:(1)成体MSC,取自骨髓、脂肪组织、外周血、牙髓等;(2) 新生儿组织来源的MSC,从胎盘、羊膜和脐带等胚胎外组织中获得[1]。
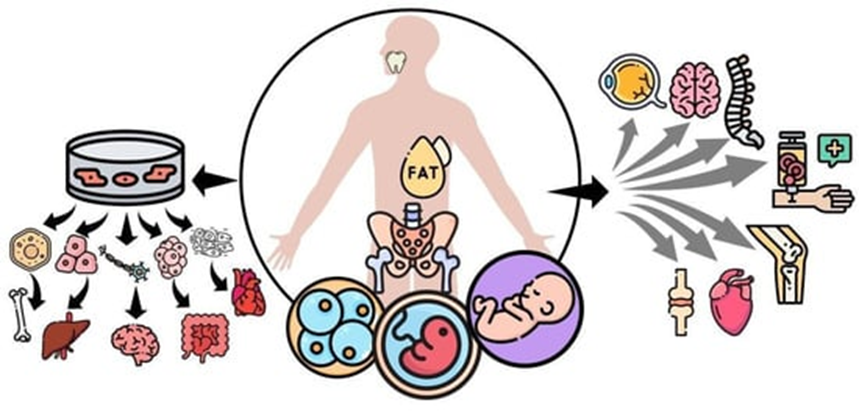
图片引用自文献1
近期,一篇名为“Mesenchymal Stem Cell Therapies Approved by Regulatory Agencies around the World”的文章发表在“Pharmaceutical”特刊“"New Advances in Mesenchymal Stromal Cells as Therapeutic Tools"上。文章通过系统回顾,分析了间充质干细胞在全球各种注册临床试验中的不同应用,并讨论了当前已获监管机构批准MSC 疗法的相关信息。

全球已经获批上市的间充质干细胞产品
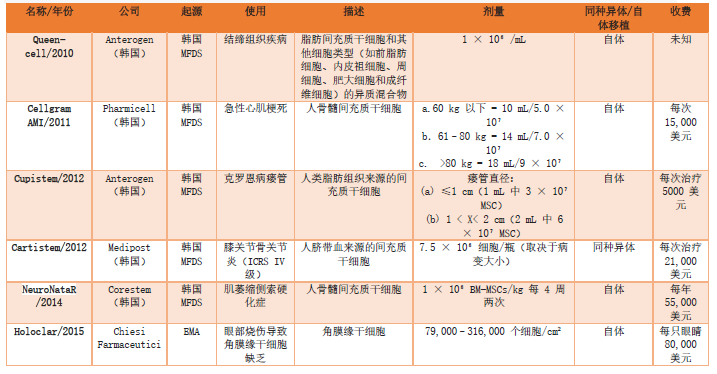
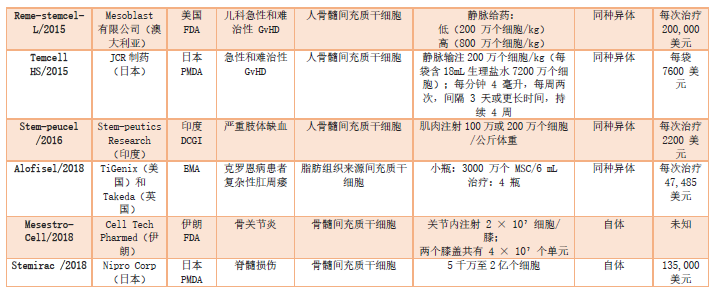
全球获批的MSCs疗法(图片引用自文献1)
目前全球范围内, 世界各地的监管机构批准的MSCs疗法共包含12项。
这些监管机构包括:欧洲药品管理局 (EMA)、美国 (USA) 食品药品管理局 (FDA)、韩国食品药品安全部 (MFDS)、印度药品监管总局 (DCGI)、澳大利亚治疗用品管理局 (TGA) 和日本药品和医疗器械管理局 (PMDA)等。
这些产品中有9种来自亚洲。
韩国包揽了其中5项:Queencell、 Cellgram-AMI、Cupistem、Cartistem 和 Neuronata-R 。
Queencell 在2010年上市,作为第一个含有MSCs的产品,获得韩国食品药品监督管理局(MFDS/KFDA)的批准,被用于治疗皮下组织缺损[5];
Cellgram-AMI是一种在急性心肌梗死(AMI)后72小时内,通过冠状动脉成形术改善左心室射血分数,实现再灌注的方法[6]。
Cupistem 用于治疗克罗恩病[5]。
Cartistem 用于治疗与骨关节炎 IV 级(分类中最严重的阶段,没有可见软骨残留)相关的膝关节软骨缺损[7]。
NeuroNata-R 具有神经保护作用,由于其抗炎和免疫调节作用,可以通过延长运动神经细胞的存活,来缓解肌萎缩侧索硬化症 (ALS) 的进展[8]。
剩下的四种产品中,两种来自日本,一种来自印度,另一种来自伊朗。
日本的产品有Temcell HS和Stemiral。
Temcell HS 是治疗急性和难治性移植物抗宿主病 (GVHD)[9]。
Stemirac 是第一个被批准用于脊髓损伤的干细胞治疗方法[10]。
印度的Stempeucel 被批准用于治疗严重肢体缺血(CLI)[11]。
伊朗的Mesestrocell 被用作骨关节炎的治疗方法 [12]。
在欧洲,迄今为止 EMA 共批准了两种 MSC 疗法。
Holoclar 用于眼部替换成人角膜上皮中受损的细胞,以治疗烧伤引起的中度至重度角膜缘干细胞缺乏症[13]。
Alofisel 被批准用于治疗成年克罗恩病患者的复杂性肛瘘[14]。
最后,美国迄今为止唯一批准的MSC疗法是Remestemcel-L,用于治疗儿科患者的难治性急性GVHD[15] 。
间充质干细胞的临床应用趋势
自 1995 年报告第一个 临床试验以来,Clinicaltrials.gov上注册的 临床试验 数量显著增加。以5年为周期来看,1995年至 2005 年期间启动了 19 项,2006 年至 2010 年期间递增到 159 个,2011 年至 2015 年期间又启动了 420 个,2016 年期间又增加了 490 个。截至 2020 年 6 月, clinicaltrials.gov上已有超过 1,138 项使用 MSC 作为治疗药物的注册 MSC 临床试验,较 2012 年列出的 220 项,10年里数量已经达5倍 [4]。
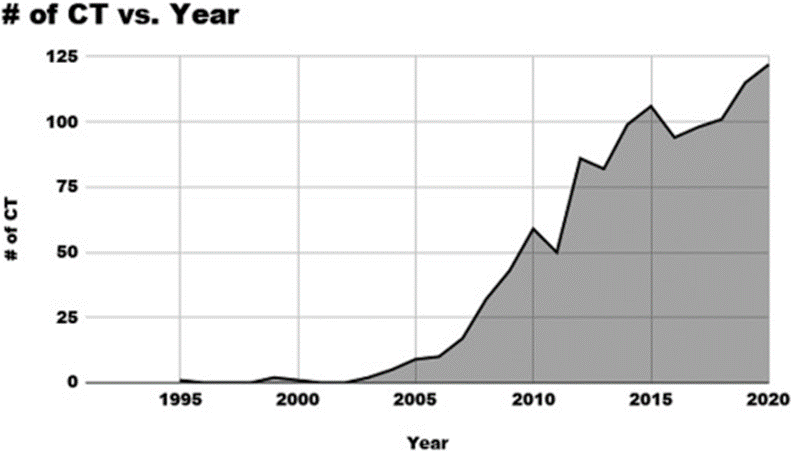
MSC临床试验注册进展(图片引用自文献4)
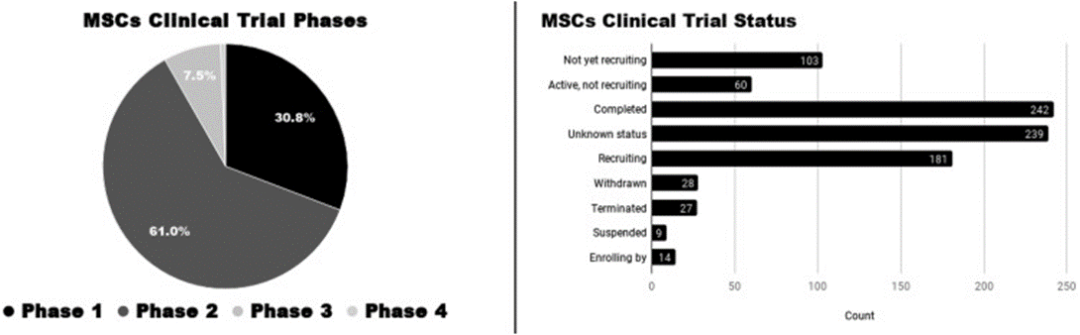
MSC临床试验注册阶段和进展分布(图片引用自文献4)
截至2020年6月,注册临床试验遍布全球51个国家。中国和美国分别以 228 个和 186 个临床试验 领先该研究。
从第二阶段选定的研究中,发表研究最多的医学专业分别是心脏病学(15项)、创伤科(6项)、呼吸科(3项)、神经科(2项)、血液科(2项)、眼科(1项)和整形外科(1项)。这些研究中有 18 项已经发表了结果。
其中,最常见的病症是膝关节炎、缺血性心脏病和扩张型心肌病。有两例病案报告了使用 MSC后,膝骨关节炎患者疼痛、僵硬和功能的临床改善;在心脏病学方面,使用 MSC被证明在临床治疗扩张型心肌病和缺血性或非缺血性心力衰竭等疾病中有效;在特发性肺纤维化患者中,注射来自胎盘的同种异体 MSC使其肺功能得到改善;在治疗脊髓损伤、乳房重建等病案中,也展示出有益结果。
未来挑战:克服间充质干细胞的异质性
大多数MSC来源于胚胎中胚层,可以从新生儿围产组织种获得。新生儿围产组织的间充质干细胞具有独特的生物学特性,例如高增殖能力、自我更新能力、更长的寿命和更大的分化潜力。

此外,仍有一部分体内的MSC起源于血管周围细胞,这些细胞不会分化成其他细胞类型来修复受损组织,而是从受损的血管中分离出来。通过其免疫调节分泌物和营养生物活性因子产生组织再生微环境,诱导其他细胞(受损组织的干细胞)进行组织再生[3]。
MSC可以从自体或同种异体来源供使用[4]。不难理解,不同来源分离的MSC在增殖方面展示出差异。令人诧异的是,从同一供体和同一来源分离的 MSC 也显示出生长速率的显着差异。
MSC的功能随着时间的推移而下降,包括增殖、集落形成、端粒长度和分化能力。一项研究表明,在第十二次分裂后,MSC克隆复杂性大大降低,从而导致弱显性克隆选择[16] 。同样,具有旁分泌作用的生物活性分子的分泌也会随着细胞分裂次数的增加而减少。

所有这些都会导致后续 MSC 克隆失去治疗潜力。克服MSCs的异质性,制造更安全稳定有效的MSC产品也是MSC疗法应用于临床的一大难题,也是未来临床需要克服的障碍。
小结
MSC疗法发展至今,其产品的临床化应用已经取得很多可喜的成绩。长远来看,将MSC扩大应用仍存在困难和阻力。除了监管机构的严格审查,MSC本身的性质也有待于进一步的深入研究。随着科技的发展和人们认识水平的提高,对待MSC疗法应持有乐观态度,让我们一起期待更多MSC产品问世。
[1] Fernández-Garza, L.E.; Barrera-Barrera, S.A.; Barrera-Saldaña, H.A. Mesenchymal Stem Cell Therapies Approved by Regulatory Agencies around the World. Pharmaceuticals 2023, 16, 1334.
[2] Naji, A.; Eitoku, M.; Favier, B.; Deschaseaux, F.; Rouas-Freiss, N.; Suganuma, N. Biological functions of mesenchymal stem cells and clinical implications. Cell. Mol. Life Sci. 2019, 76, 3323–3348.
[3] Guimarães-Gamboa, N.; Cattaneo, P.; Sun, Y.; Moore-Morris, T.; Gu, Y.; Dalton, N.D.; Rockenstein, E.; Masliah, E.; Peterson, K.L.; Stallcup, W.B.; et al. Pericytes of Multiple Organs Do Not Behave as Mesenchymal Stem Cells In Vivo. Cell Stem Cell 2017, 20, 345–359.
[4] Rodríguez-Fuentes, D.E.; Fernández-Garza, L.E.; Samia-Meza, J.A.; Barrera-Barrera, S.A.; Caplan, A.I.; Barrera-Saldaña, H.A. Mesenchymal Stem Cells Current Clinical Applications: A Systematic Review. Arch. Med. Res. 2021, 52, 93–101.
[5] Ministry of Food and Drug Safety. Biological Products (Cell therapy products) ANTEROGEN. Available online: https://www.mfds.go.kr/eng/brd/m_30/view.do?seq=71337&srchFr=&srchTo=&srchWord=&srchTp=&itm_seq_1=0&itm_seq_2=0&multi_itm_seq=0&company_cd=&company_nm=&page=1
[6] PHARMICELL. Business (Stem Cell Drugs) Hearticellgram-AMI is the World’s First Stem Cell Drug. Available online: http://www.pharmicell.com/eng/biz/medicine_cellgram.html
[7] CARTISTEM. Products (1st Generation). Available online: https://www.medi-post.com/cartistem
[8] CORESTEM (Products) ALS (NeuroNata-R). Available online: http://corestem.com/en/m21.php
[9] BioPharma Asia (Sections). JCR Pharma Launch TEMCELL HS in Japan. Available online: https://biopharma-asia.com/sections/jcr-pharma-launch-temcell-hs-in-japan/
[10] Cyranoski, D. Japan’s approval of stem-cell treatment for spinal-cord injury concerns scientists. Nature 2019, 565, 544–545.
[11] Stempeutics (Products) Stempeucel. Available online: https://www.stempeutics.com/stempeucel.html
[12] CellTech Pharmed. Mesestrocell: Cell Therapy for Osteoarthritis. Available online: http://en.celltech.ir/
[13] European Medicine Agency Sciences Medicine Health (Medicines). Holoclar. Available online: https://www.ema.europa.eu/en/medicines/human/EPAR/holoclar#:~:text=Holoclar%20is%20a%20stem%2Dcell,iris%20(the%20coloured%20part)
[14] European Medicine Agency Sciences Medicine Health (Medicines). Alofisel. Available online: https://www.ema.europa.eu/en/medicines/human/EPAR/alofisel
[15] Oncology Drugs Advisory Committee. Remestemcel-L for Treatment of Steroid Refractory Acute Graft Versus Host Disease in Pediatric Patients; FDA Advisory Committee: Washington, DC, USA, 2020; pp. 1–127.
[16] Wilson, A.; Hodgson-Garms, M.; Frith, J.E.; Genever, P. Multiplicity of Mesenchymal Stromal Cells: Finding the Right Route to Therapy. Front. Immunol. 2019, 10, 1112.
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
