




恶性肿瘤一直以来都是人类不断攻克的难关,但目前,一直未找到能够终结恶性肿瘤的根治性手段。虽然手术、化疗、放疗是目前恶性肿瘤最主要的治疗手段,但仍抵挡不住寻求更加有效的治疗方法。免疫细胞治疗的问世,让人类“攻克”恶性肿瘤又向前迈进了一步。
2022年,免疫细胞治疗恶性肿瘤在全球各国逐渐扩大应用,并形成了一些专家共识及实践建议。
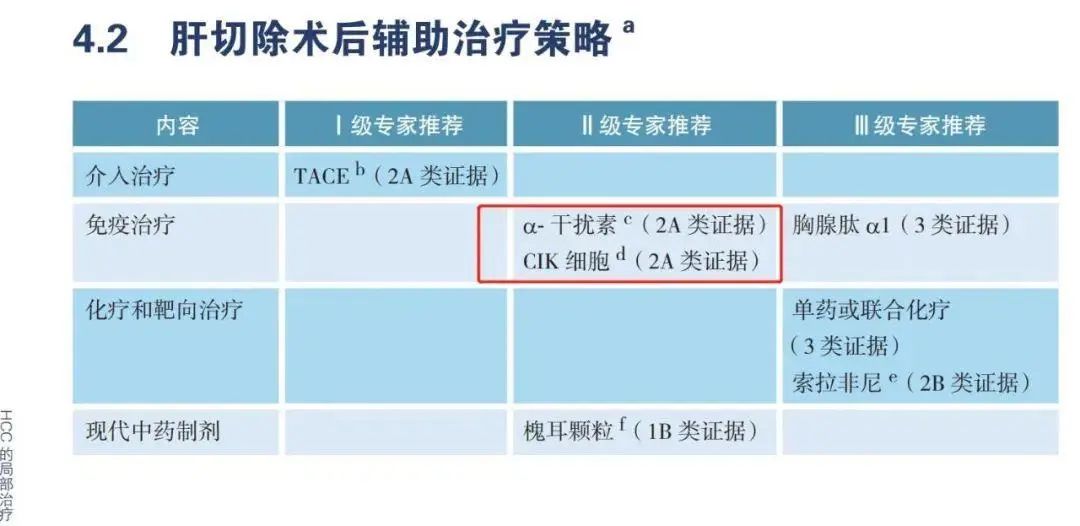
在我国,根据《CSCO原发性肝癌诊疗指南2022版》,CIK细胞疗法写进了肝切除术后辅助治疗推荐方案(证据水平:2A类)。

在国际上,欧洲联合起草了CAR-T临床实践建议。欧洲血液和骨髓移植学会联合认证委员会和欧洲血液学协会等专家,基于当前的文献数据,更新了关于成人/儿童CAR-T的临床最佳实践建议,内容包括从患者筛选到长期随访、给药后安全检测和监管全流程,期望支持医疗人员在这一快速发展的领域提供一致、高质量的治疗。

这些均意味着,免疫细胞治疗正在开启恶性肿瘤治疗方法的革命性新时代。
当前,CAR-T免疫细胞是最为热门的一类肿瘤免疫疗法,是最具有代表性的恶性肿瘤革命性疗法之一。今天,我们可以通过发表在《Biomed pharmacother》上的一篇研究[1],来全面了解CAR-T细胞治疗恶性肿瘤治疗的最近进展,以及正在面临的机遇、局限与挑战。

历经五代,CAR-T细胞以更强的实力攻克恶性肿瘤
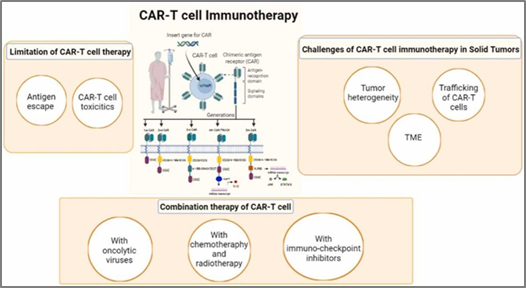
图1(图片源于[1])
CAR-T细胞实则为一种工程化的T细胞,它是利用基因工程技术给从恶性肿瘤患者身上分离出来的免疫T细胞,加入一个能够识别肿瘤细胞,并且同时激活T细胞杀死肿瘤细胞的嵌合抗体。此时,T细胞就变成了CAR-T细胞。CAR-T细胞能够在体内找到肿瘤细胞,并激活机体免疫功能,发动自身免疫,杀死肿瘤细胞。
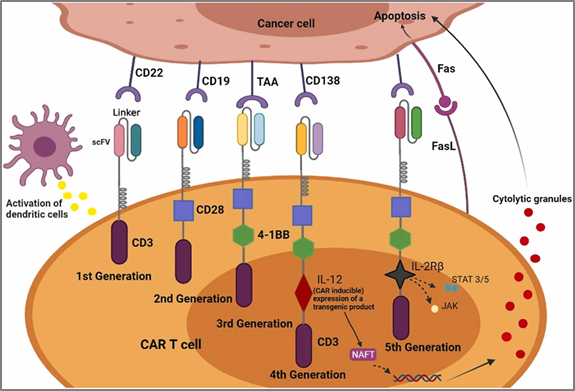
图2(图片源于[1])
目前,已经培育出了5代CAR-T细胞,其中第5代CAR-T细胞比前几代多了一个额外的细胞内结构域。因此,其分泌的信号不仅可以驱动CAR-T细胞保持活性并产生记忆T细胞,而且还能够重新激活和刺激免疫系统。
CAR-T细胞疗法往往需要数周时间,CAR-T细胞被回输到患者的循环系统后,它们可以帮助捕获肿瘤细胞上的特定抗原,并在它们开始与肿瘤细胞结合后将其摧毁,进而实现杀死肿瘤细胞的目的。
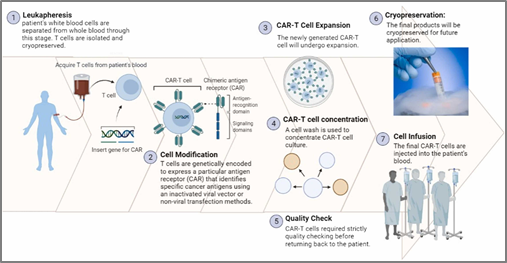
图3(图片源于[1])
CAR-T细胞疗法面临的挑战
目前, CAR-T细胞疗法在血液系统恶性肿瘤中取得巨大的成功,同时许多人尝试使用这种疗法治疗实体瘤。迄今为止,针对多种实体瘤的CAR-T细胞疗法已经进行了许多临床前研究和临床试验,包括胶质母细胞瘤、神经母细胞瘤、乳腺癌、胰腺导管腺癌、结直肠癌、消化道肿瘤等。
然而,CAR-T在恶性肿瘤领域的应用仍然面临着诸多挑战。
(1)毒副作用:CAR-T细胞疗法并不完全安全,这是其目前存在的最关键的局限性。尽管CAR-T细胞疗法取得了巨大的成就,但是无法回避的是它可预期和意外毒性的发生,如细胞因子释放综合征(CRS) ,其通常在CAR-T细胞注射后的前几周出现,CRS可导致促炎细胞因子增加,使机体发生从轻微的感冒样疾病到可能致命的严重多器官衰竭等不良事件。
免疫效应细胞相关神经毒性综合征(ICANS)是CAR-T细胞治疗患者的另一种常见毒性,其特征包括意识模糊、谵妄、失语、肌阵挛和癫痫发作。ICANS的发生率因疾病而异,急性淋巴细胞白血病患者出现ICANS的几率约为40-62%,而淋巴瘤患者的发生ICANS的几率为23-67%。
(2)抗原异质性与免疫逃逸:细胞治疗成功的第一步是选择合适的靶抗原,但由于肿瘤细胞具有高度的抗原异质性,T细胞对靶细胞的识别能力受损。另外,部分接受CAR-T细胞治疗的患者的肿瘤细胞仅仅表达出部分甚至不表达靶抗原。这样,也就大大增加了CAR-T细胞寻找肿瘤细胞的难度,成为了CAR-T细胞疗法长期可行性的关键问题。

(3)CAR-T细胞治疗实体肿瘤疗效仍较低:
与血液肿瘤相比,实体瘤的细胞治疗结果并不令人满意。其主要原因与实体肿瘤的特殊性有关。
一方面是由于实体肿瘤的内皮细胞中黏附分子表达不足,同时肿瘤部位的趋化因子表达与CAR-T细胞表面的趋化因子受体不匹配。
另一方面是由于实体肿瘤内致密的肿瘤相关成纤维细胞严重阻碍了CAR-T细胞的浸润。正是以上两种因素降低了CAR-T细胞疗法的疗效。
CAR-T细胞治疗的新策略
那么,如何攻克CAR-T疗法面临的上述障碍呢?联合疗法是关键,很多研究都在关注联合疗法,以增加CAR-T细胞治疗实体恶性肿瘤的有效性。
(1)FDA批准的唯一一种溶瘤病毒(OV)
T-VEC是FDA批准的唯一一种由1 型单纯疱疹病毒(HSV-1) 产生的溶瘤病毒(OV),OV一方面可以直接裂解肿瘤细胞和产生抗肿瘤适应性免疫,另一方面可以增强T细胞的适应性活性,进而与CAR-T细胞发挥协同作用共同克服实体恶性肿瘤。
(2) 放化疗、单克隆抗体联合治疗
已有研究表明,化疗药物如环磷酰胺、多柔比星、氟尿嘧啶等可通过多种机制提高CAR-T细胞治疗的有效性。放射治疗也可以通过增加肿瘤抗原的表达以及趋化因子的释放来促进CAR-T细胞的浸润。而单克隆抗体与CAR-T细胞联合治疗可以防止CAR-T细胞衰竭并维持其功效。
目前,全球已经有8款CAR-T免疫细胞治疗治疗获批上市,但CAR-T细胞疗法在治疗恶性肿瘤方面存在有很多挑战。近年来,由于新一代CAR-T细胞疗法在治疗血液系统恶性肿瘤方面显现出了显著的疗效,在恶性肿瘤治疗领域引起了极大的轰动,也让我们看到了治疗恶性肿瘤的一个新希望。未来,也希望更多的临床试验给我们带来有关CAR-T细胞治疗恶性肿瘤的实质性进展。
参考文献
[1] Ali Zar,et al.Therapeutic potential of CAR T cell in malignancies: A scoping review[J].Biomedicine & Pharmacotherapy,2022. https://pubmed.ncbi.nlm.nih.gov/34894519/.
[2] H. Zhao, et al.Inflammation and tumor progression: signaling pathways and targeted intervention[J].Signal Transduct. Target. Ther., 6 (1) (2021), p. 263.https://api.mendeley.com/cross_publisher_access/v2/link_resolver.
本文为知识性科普,仅供学习、交流,请勿用作商业用途。
相关新闻
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
