




本文重点摘要
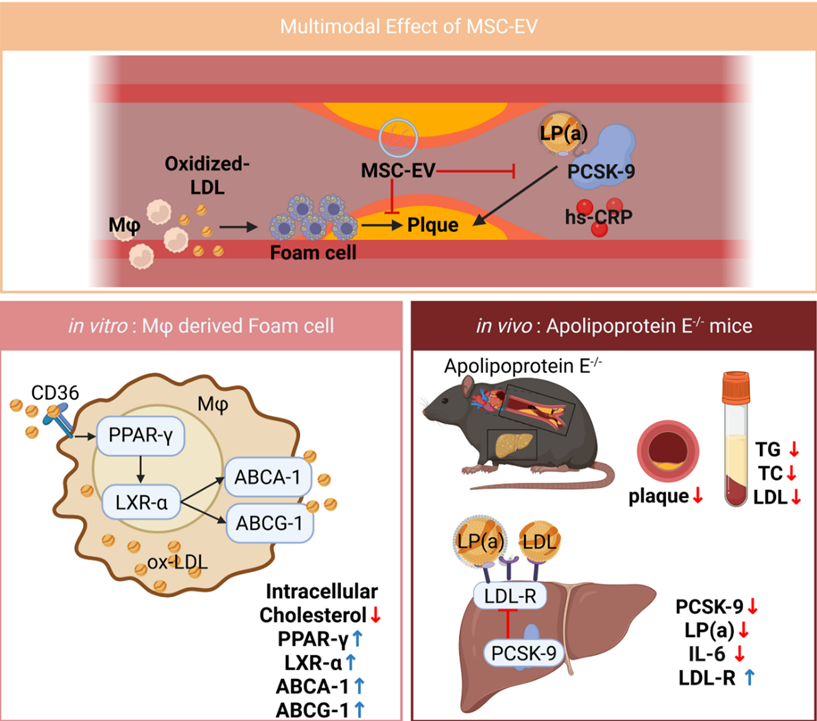
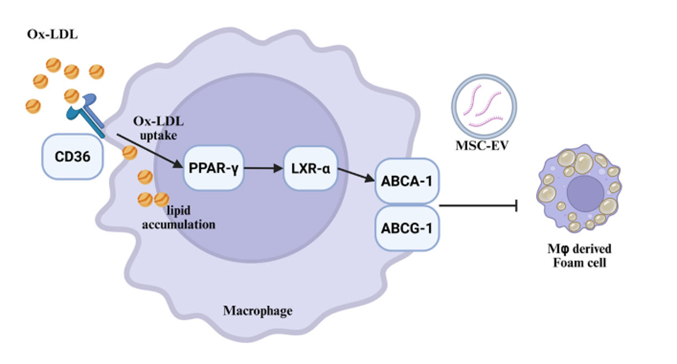
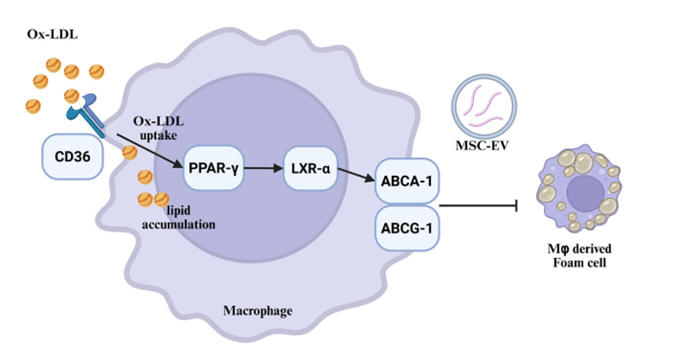
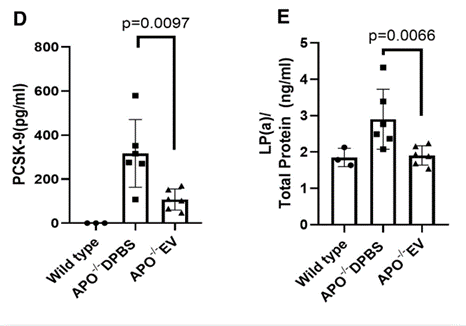
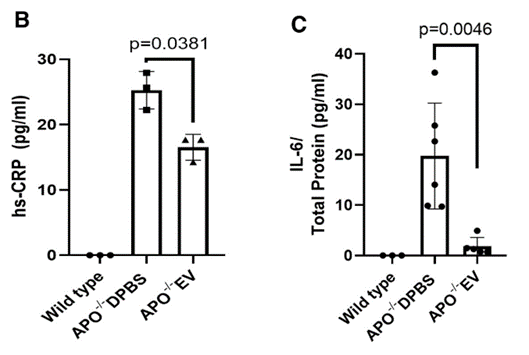
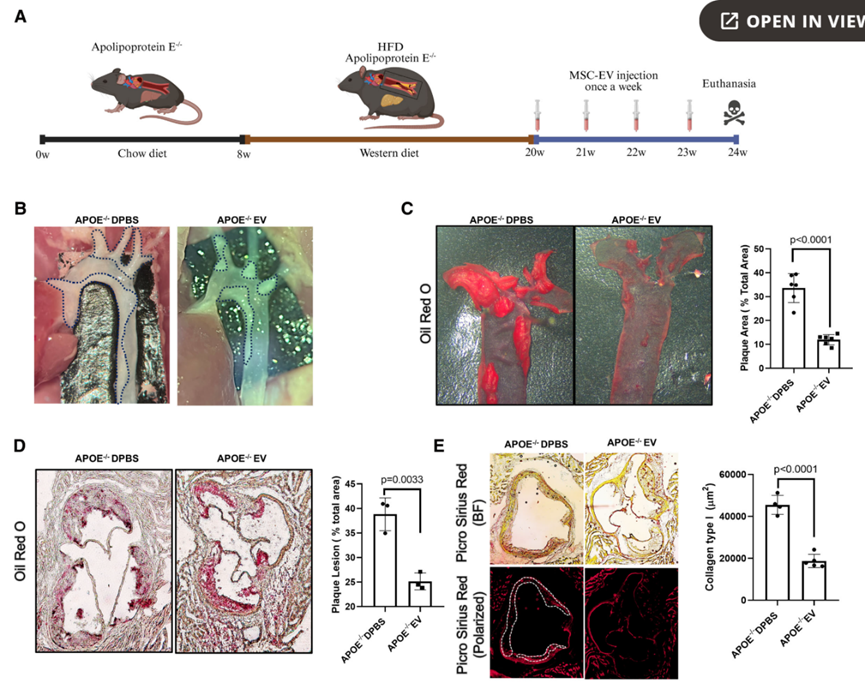
近期,间充质干细胞来源细胞外囊泡(MSC-EVs)的研究进展为动脉粥样硬化(AS)患者的治疗带来了新希望,根据最新研究报道: (1)临床级MSC-EVs采用静脉输注方式,可直接靶向血管病变部位,轻松穿透血管壁屏障,将其负载的生物活性物质(蛋白质、脂质、mRNA及microRNA等)输送到受损的血管内皮细胞、巨噬细胞及炎性免疫细胞。 (2)静脉输注MSC-EVs与传统方案(如他汀类药物、PCSK9抑制剂)相比具有多重优势,如靶向性强、生物利用度高,无免疫排斥及无致瘤风险,操作便捷微创,患者依从性高,伦理争议少,可实现多靶点协同干预。 (3)MSC-EVs因其能够增强胆固醇流出、抑制PCSK9和Lp(a)水平、减少全身炎症反应,并修复受损血管内皮组织,延缓动脉粥样硬化斑块进展,成为治疗动脉粥样硬化的一种有前途的无细胞治疗方法。 动脉粥样硬化(AS)作为心脑血管疾病的“隐形杀手”,悄无声息地损伤血管、堵塞管腔,最终诱发心梗、脑梗等致命并发症。 据《柳叶刀》子刊研究估算[2],全球动脉粥样硬化患病人数已近20亿,我国患病人数超2.7亿! 近期,国际权威研究《Multimodal Antiatherosclerotic Effects of Clinical-Grade Mesenchymal Stem Cell-Derived Extracellular Vesicles》一文发布,深入解析间充质干细胞来源细胞外囊泡(MSC-EVs)抗动脉粥样硬化的核心机制与治疗潜力,为解决这一全球性健康难题提供了新思路。 不同于传统降脂、抗炎药物“治标不治本”的局限, MSC-EVs作为临床级无细胞治疗载体,凭借多模态干预优势,在动脉粥样硬化的预防、干预与逆转中展现出独特价值。 动脉粥样硬化,为何成为“全球健康杀手”? 动脉粥样硬化并非突发疾病,而是一个长期、缓慢的病理过程——以血管内皮损伤为始动环节,脂质沉积、炎症浸润、斑块形成、血管狭窄为核心进程,最终导致血管失去弹性、管腔堵塞,引发心脑血管事件。 其核心诱因包括高胆固醇、高血脂、高血压、糖尿病、肥胖及不良生活习惯等,而传统治疗多依赖他汀类药物、PCSK9抑制剂等,仅能暂时控制血脂水平,无法修复受损血管内皮、逆转已形成的动脉斑块,且长期用药易产生耐药性、肝肾损伤等副作用。 该研究明确指出[1],动脉粥样硬化的本质是“脂质代谢紊乱+全身慢性炎症”的双重失衡,而MSC-EVs恰好能通过多靶点、多途径干预,从根源上打破这一病理循环,为临床治疗提供了全新思路。 图片来自文献[1] 外泌体抗动脉粥样硬化的3大关键机制 该研究通过体外细胞实验、体内动物模型验证,明确了MSC-EVs抗动脉粥样硬化的三大核心机制,均围绕“脂质调控+炎症抑制+血管修复”展开,精准直击疾病根源。 机制一:增强胆固醇流出,阻断脂质沉积 脂质沉积是动脉粥样硬化斑块形成的核心前提,其中巨噬细胞吞噬氧化型低密度脂蛋白(ox-LDL)后形成泡沫细胞,是斑块脂质核心的主要来源,而胆固醇外流障碍则会加速泡沫细胞堆积。 该研究证实[1],MSC-Evs可通过携带的多种活性microRNA,靶向激活巨噬细胞内ATP结合盒转运子A1(ABCA-1)、G1(ABCG-1)等胆固醇转运蛋白表达,抑制ABCA-1/G1的负调控因子(如LRP1、IDOL),从而增强胆固醇从巨噬细胞向高密度脂蛋白(HDL)的外流效率,减少泡沫细胞形成与脂质沉积,从源头延缓斑块进展。 简单来说,MSC-EVs就像“血管清道夫”,能帮助血管内多余的胆固醇“排出体外”,避免其堆积形成斑块。 图片来自文献1 机制二:抑制PCSK9与Lp(a),调控血脂平衡 PCSK9(前蛋白转化酶枯草溶菌素9)和Lp(a)(脂蛋白a)是动脉粥样硬化的关键危险因素: PCSK9会降解肝细胞表面的低密度脂蛋白受体(LDLR),降低肝脏对血液中低密度脂蛋白(LDL)的清除能力,导致“坏胆固醇”升高; Lp(a)则会促进脂质沉积、加速血管钙化,且传统降脂药物对其调控效果有限。 该研究首次明确[1],临床级MSC-EVs可通过其携带的蛋白质和microRNA等,双重抑制PCSK9的表达与活性,减少LDLR的降解,增强肝脏对LDL的清除能力;同时,MSC-EVs能显著降低血清中Lp(a)水平,此外,TC、甘油三酯和LDL-C水平也显着降低,而HDL-C水平保持不变。 这弥补了传统药物的短板,实现血脂的全面调控,进一步降低动脉粥样硬化的发病风险。 图片来自文献[1] 机制三:减少全身炎症,修复血管内皮 慢性全身炎症是动脉粥样硬化进展的核心驱动力,血管内皮损伤则是疾病的始动环节——炎症因子(如TNF-α、IL-6)会持续损伤血管内皮,导致血管通透性增加,加速脂质渗透和炎症细胞浸润,形成“炎症-损伤-沉积”的恶性循环。 该发现,MSC-EVs可通过携带的抗炎蛋白和多种活性分子,靶向抑制多条炎症通路,下调TNF-α、IL-6等促炎因子表达,同时上调IL-10等抗炎因子水平,诱导巨噬细胞从促炎M1型向抗炎M2型极化,减少全身炎症反应。 同时,MSC-EVs可靶向修复受损血管内皮细胞,促进内皮细胞增殖迁移,上调一氧化氮合酶表达,改善血管舒张功能,重建血管内皮屏障,阻止脂质和炎症细胞进一步浸润,实现“抗炎+修复”双重作用,延缓血管狭窄进程[1]。 图片来自文献[1] 以上三大关键机制的共同作用下,最终使得MSC-Evs的抗动脉粥样硬化作用显著,在小鼠动物模型研究中发现[1]: MSC-Evs治疗组的脂质动脉粥样硬化斑块沉积明显减少,通过相关染色显示,MSC-Evs治疗组动脉壁中的胶原沉积,特别是I型胶原减少,表明纤维化重塑减少。 小结 MSC-EVs以“无细胞、高安全、多靶点、易普及”的独特优势,打破了动脉粥样硬化“难以逆转、长期依赖药物”的临床困局。MSC-EVs通过增强胆固醇流出、抑制PCSK9和Lp(a)、减少全身炎症等多模态干预优势,从根源上干预疾病进程,规避了传统药物的副作用。随着临床级制备技术的不断完善、临床研究的持续推进,相信在不久的将来,MSC-EVs将有望成为动脉粥样硬化干预的新选择,为全球心脑血管健康保驾护航,让更多人远离心梗、脑梗的致命威胁。 本期撰文:福建医科大学 YANG 本文审核专家:江苏大学附属医院 李晶教授 参考文献: [1]Kim J, Park D, Yoo J, Kim JE, Kim EH, Bang OY. Multimodal Antiatherosclerotic Effects of Clinical-Grade Mesenchymal Stem Cell-Derived Extracellular Vesicles. Stroke. 2026;57(4):1008-1021. doi:10.1161/STROKEAHA.125.052894 [2] Song P, Fang Z, Wang H, et al. Global and regional prevalence, burden, and risk factors for carotid atherosclerosis: a systematic review, meta-analysis, and modelling study. Lancet Glob Health. 2020;8(5):e721-e729. doi:10.1016/S2214-109X(20)30117-0

相关新闻
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
