




引言
今日分享一则跟干细胞及其衍生物改善疤痕相关的综述。这篇综述包括了43项研究,证明了脂肪来源干细胞及其衍生物产品(包括干细胞、外泌体等)改善病理性瘢痕的潜力。
干细胞及其衍生物产品通过调节细胞外基质、促进血管生成以及减少增生性瘢痕和瘢痕疙瘩的炎症反应,从而改善瘢痕质地。
干细胞及其衍生物产品还可以防止萎缩性瘢痕中的胶原蛋白降解。
干细胞及其衍生物产品在与点阵CO2激光、PRP、肉毒杆菌毒素和光调等方法相结合时也显示出潜力,且单药或联合使用时的疗效各不相同。
瘢痕,这道刻在皮肤上的印记,不仅是美观问题,更是无数患者的难言之痛。
在医学领域,病理性瘢痕包括增生性瘢痕、瘢痕疙瘩和萎缩性瘢痕,它们源于伤口愈合过程中细胞外基质重塑失衡、炎症反应失调和成纤维细胞异常调控。
传统治疗如激素注射、激光治疗和手术修复效果参差不齐,复发率居高不下。
近年研究表明,干细胞及其衍生物相关技术及产品正逐渐成为解决这一难题的新希望。
2025年5月发表在《Clinical, Cosmetic and Investigational Dermatology》上的一篇综述[1]系统分析了这一领域的最新进展,为瘢痕治疗带来了突破性视角。

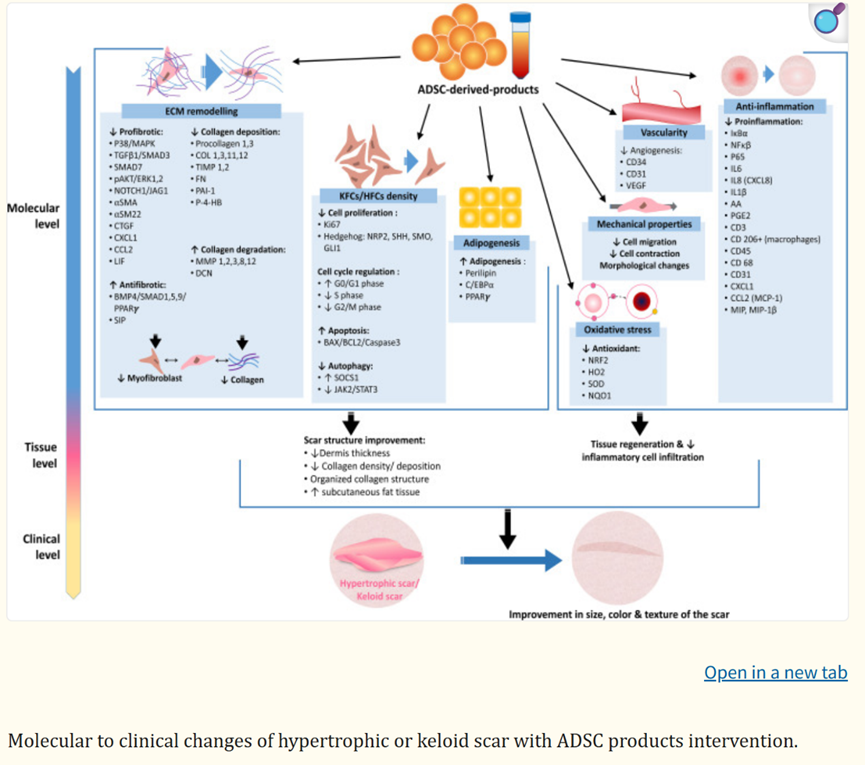
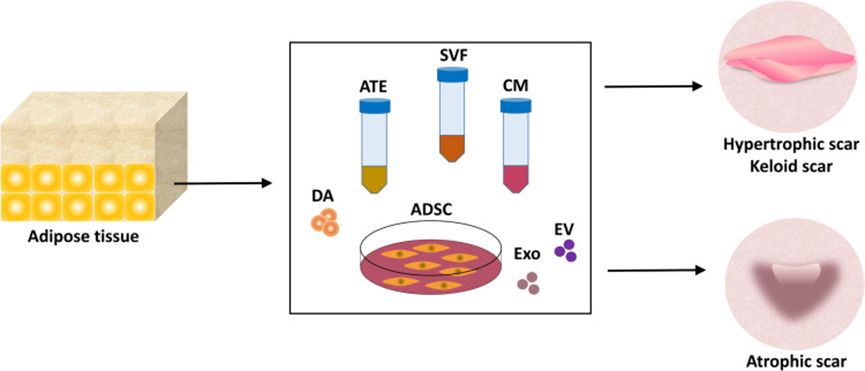
01 瘢痕的形成 皮肤损伤后的愈合是一个复杂而精密的生物学过程,正常瘢痕形成遵循严格的四阶段模式:血肿形成、炎症、增殖和重塑。然而当这一过程出现偏差,便会催生病理性瘢痕。 增生性瘢痕通常局限于原始伤口范围内,呈现红肿、坚硬的外观,伴有瘙痒和疼痛。它们在伤后4-8周内形成并扩展,随后趋于稳定。 相比之下,瘢痕疙瘩则具有“侵略性”,它们会突破伤口边界,像肿瘤一样向周围健康组织蔓延,可能在伤后数月甚至数年才显现。更令人惊讶的是,瘢痕疙瘩中的胶原产量是正常皮肤的20倍,其纤维连接蛋白生物合成是正常瘢痕的4倍。这种过度生长不仅影响外观,还常导致皮肤收缩和功能障碍。 萎缩性瘢痕则走向另一极端——胶原降解过度,形成凹陷的皮肤表面。无论哪种类型,病理性瘢痕都严重影响着患者的生活质量和心理健康! 02 干细胞及其衍生物改善瘢痕的机制 干细胞因其易获取、多向分化潜能和强大旁分泌能力,成为瘢痕治疗的新星。 图片来自文献1 根据最新研究,干细胞及其衍生物构成的技术及产品可分为两大类——细胞疗法(干细胞)和无细胞疗法(分泌组、外泌体等)。这些技术及产品通过多种机制改善病理性瘢痕: 干细胞及其衍生物改善病理性瘢痕的机制[1] 1.调控细胞外基质(ECM):干细胞及其衍生物能平衡胶原合成与降解,减少过度纤维化。在增生性瘢痕和瘢痕疙瘩中,它们降低过度沉积的胶原;而在萎缩性瘢痕中,它们则防止胶原过度降解。 2.促进血管新生:干细胞分泌的血管内皮生长因子(VEGF)等因子能改善瘢痕组织血液供应。研究表明,脂肪移植可选择性增加瘢痕组织血管密度,使微血管结构正常化。 3.抑制炎症反应:干细胞及其衍生物能调节巨噬细胞从促炎的M1型向抗炎修复的M2型转化,减轻慢性炎症状态。 4.影响关键信号通路:干细胞及其衍生物通过下调TGF-β1/Smad通路抑制成纤维细胞过度活化,同时促进TGF-β3表达。—后者被证明能减少瘢痕形成而不降低伤口抗拉强度。 03干细胞及其衍生物改善瘢痕的临床进展 该综述通过全面的文献检索,综合分析了利用干细胞及其衍生物相关的治疗病理学瘢痕的临床前研究及临床研究。 在纳入的临床前研究中,6项研究使用了动物来源的干细胞及其衍生物,28项研究使用了人类来源的干细胞及其衍生物作为瘢痕疙瘩或肥大细胞或组织模型的干预措施。在临床前试验中没有发现使用萎缩性瘢痕模型的研究。 该研究还分析了6项临床试验,包括43名患有增生性瘢痕的受试者,8名患有瘢痕疙瘩的受试者,和73例萎缩性瘢痕受试者。 图片来自文献[1] 临床前研究:在动物瘢痕模型中,注射干细胞及其条件培养基均显示α-SMA和I型胶原mRNA表达减少,胶原沉积减少且排列更有序。值得注意的是,干细胞在瘢痕组织内可长期存活,其抑制瘢痕增生挛缩的效果优于单纯使用条件培养基。 临床研究:在临床研究中,瘢痕位置、患者年龄和瘢痕类型显著影响干预效果,疗效有个体化差异。 04 干细胞联合其他技术,成为改善瘢痕的新热点 单一疗法在复杂病理性瘢痕面前常显不足,联合治疗策略正成为临床研究热点: 激光联合治疗:点阵CO2激光与干细胞及其衍生物联用可产生协同效应。激光在皮肤上创造微通道,不仅促进干细胞及其衍生物渗透,其热刺激还能激活皮肤修复机制。研究表明,联合疗法在改善瘢痕颜色、质地和弹性方面优于单一治疗。 富血小板血浆(PRP)增强:PRP富含多种生长因子,与干细胞联用可显著提高脂肪移植物存活率。PRP提供“营养基”,延长干细胞在瘢痕局部的存活和功能发挥时间。 经皮针刺筋膜切开自体脂肪移植术(PALF):这项技术创新性地使用针尖松解瘢痕组织及皮下纤维化粘连,创建蜂巢状组织腔隙,再注入富含干细胞的自体脂肪。研究表明,PALF能将限制性瘢痕转化为可接受脂肪移植的疏松三维受体再生基质,显著改善成熟瘢痕的质地、外观和弹性。 生物材料搭载:直接注射干细胞存在存活率低、易流失的问题。目前诸多研究正在开发负载干细胞产品的各种生物材料,旨在实在其持续释放。 小结 干细胞及其衍生物如同天然的“修复调节器”,通过平衡胶原代谢、抑制过度炎症、促进血管新生及调控关键信号通路,从根源上干预疤痕形成的病理过程。当前临床研究与初步实践已证实其在改善疤痕外观、质地及症状方面的潜力。未来,个体化方案优化、工程化外泌体修饰以及更长效稳定剂型的开发,将成为推动这一技术从实验室迈向广泛应用的关键。 参考文献: [1] Alfarafisa NM, Chou Y, Santika R, Riestiano BE, Soedjana H, Syamsunarno MRAA. Adipose-Derived Stem Cell Products and Combination Therapies for the Treatment of Pathological Scars: A Review of Current Preclinical and Clinical Studies. Clin Cosmet Investig Dermatol. 2025;18:1309-1337. Published 2025 May 27. doi:10.2147/CCID.S511067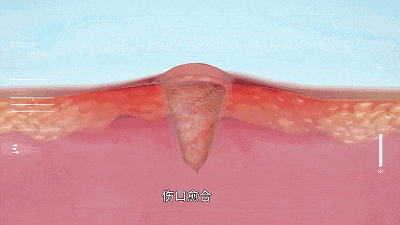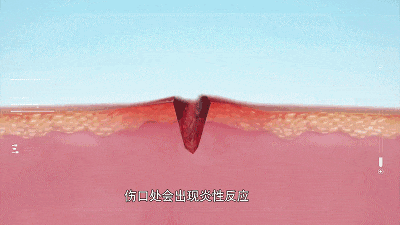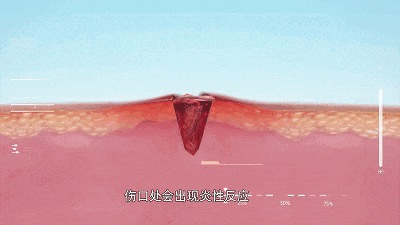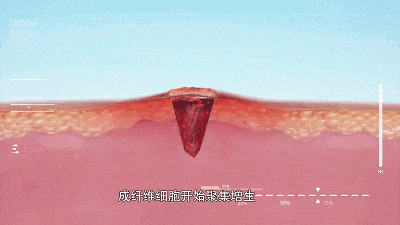

相关新闻
博雅新闻
行业政策

在线咨询
留言您的联系方式及需求,专业顾问将于收到资料后尽快与您回复。
我要预约
填写您的预约需求,您将获得相应的专业顾问满足您的需求。
电话咨询
全国统一客服专线400-885-0012,期待为您服务。
微信咨询
直接添加客服微信号,专业顾问随时准备解答您的一切疑问。
在线咨询



服务热线
400-885-0012


官方微信



TOP

观望只会错过守护宝宝和家庭的机会
存储新生儿干细胞
机会一生只有一次

扫码了解细胞新时代
